Mais de 8 milhões de bebês nasceram com essa tecnologia só nos Estados Unidos
Se você falar com um grupo de 100 pessoas nascidas nos Estados Unidos, é provável que duas delas tenham nascido como resultado de Fertilização in Vitro (FIV), de acordo com o Zev Williams, diretor do Centro de Fertilidade da Universidade de Columbia.
“Em muitos aspectos, a Fertilização in Vitro é na verdade um dos grandes triunfos dae mdicina moderna (…) Uma coisa que é útil saber é o quão comum ela é. Cerca de 2% dos nascimentos nos EUA são resultado de Fertilização in Vitro: mais de 8 milhões de bebês nasceram com essa tecnologia”, afirma.
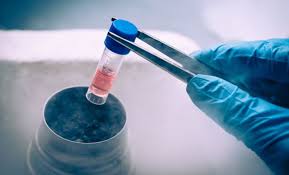
Outra tecnologia importante para o processo de Fertilização in Vitro é a criopreservação do embrião, que é o congelamento após a fertilização do óvulo. A Suprema Corte do Alabama decidiu na última sexta-feira (16) que embriões congelados são crianças e seriam protegidos pela Lei estadual de Morte Injusta de uma Criança.
A decisão sem precedentes da Suprema Corte do Alabama sobre embriões congelados pode afetar os tratamentos de Fertilização in Vitro, alertam os críticos. Enquanto os especialistas em infertilidade alertam sobre o impacto da reprodução assistida falhada, outros especialistas falaram com a CNN para compartilhar o que as pessoas devem saber sobre a Fertilização in Vitro e o congelamento de óvulos.
O que é Fertilização in Vitro?
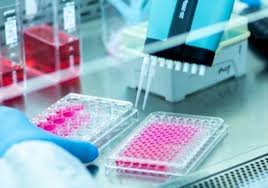
A Fertilização in Vitro ocorre quando um óvulo é removido do corpo de uma mulher e combinado com o esperma em um laboratório antes de ser implantado, explica Eve Feinberg, professora associada de obstetrícia e ginecologia na Feinberg School of Medicine, Northwestern University.
Para conseguir isso, os pacientes são submetidos a injeções de fertilidade de oito a 10 dias com hormônios que ajudam seus óvulos a amadurecerem, diz Mamie McLean, especialista em infertilidade da Alabama Fertility em Birmingham. Os procedimentos de retirada de óvulos são realizados em regime ambulatorial ou hospitalar e, às vezes, sob sedação consciente, acrescenta McLean.
Após a fertilização, os médicos observam o desenvolvimento dos embriões. Feinberg diz que o que se vê com frequência é que a reprodução humana é realmente ineficiente.
Se 10 óvulos forem expostos ao esperma, cerca de sete serão fertilizados, observa ele. Desses sete, apenas 25% a 50% crescerão em laboratório por tempo suficiente para serem considerados um embrião mais maduro chamado blastocisto, acrescenta Feinberg.
A partir daí, dependendo da idade do paciente, o blastocisto tem entre 10% e 60% de chance de virar bebê, afirma.
Quando a Fertilização in Vitro é útil?
A Fertilização in Vitro foi desenvolvida pela primeira vez na década de 1970 para ajudar mulheres que bloquearam as trompas de falópio, a parte do sistema reprodutivo onde convergem o espermatozoide e o óvulo, diz McLean.
Desde então, foi expandido para ajudar a concepção em muitos outros contextos, como para pessoas com abortos recorrentes, infertilidade masculina, aquelas que utilizam barriga de aluguel e aquelas para quem outros tratamentos de fertilidade falharam, acrescenta. “É o nosso tratamento de maior sucesso”, diz McLean.
A tecnologia também permitiu que casais com doenças genéticas testassem os seus embriões e transferissem apenas aqueles que não seriam afetados por essas doenças, diz Williams.
Por que congelar embriões?
Congelar embriões é útil para testes genéticos, diz Feinberg.
Os médicos coletam amostras de células de embriões para testá-los em busca de doenças ou anomalias genéticas, mas esses testes podem levar de duas a quatro semanas para serem realizados, observa ele. Enquanto isso, o congelamento dos óvulos os mantém viáveis enquanto os profissionais de saúde investigam os fatores genéticos.
As pacientes também podem optar por congelar os embriões quando não pretendem engravidar imediatamente, explica Feinberg. Geralmente há taxas de sucesso mais altas quando os embriões fertilizados são congelados, e não apenas o óvulo, acrescenta.
Também podem fazer a FIV por razões médicas, como antes da quimioterapia para o tratamento do câncer, que pode danificar os ovários. Ou também porque não estão na fase certa da vida para conceber, mas querem ter mais hipóteses de engravidar no futuro, diz Feinberg.
Se um ciclo de Fertilização in Vitro resultar em vários embriões, congelá-los pode manter aqueles que não foram implantados viáveis para uso futuro, diz McLean.
E embora no passado fosse comum implantar vários embriões, o congelamento de embriões permite aos médicos preservarem os outros para uso futuro, para que um embrião possa ser implantado de cada vez, o que é muito mais seguro para o paciente e para o futuro bebê, explica Williams.
Por que não fertilizar apenas um óvulo?
“A ciência por trás da Fertilização in Vitro realmente mostra que um único óvulo fertilizado não é suficiente”, diz Feinberg.
Se as suas pacientes dizem que querem dois ou três filhos, Feinberg incentiva o congelamento de dois a quatro embriões para cada um, diz ele.
Quando um embrião congelado é aquecido para implantação, há uma taxa de sobrevivência de cerca de 95%, o que significa que 5% não sobreviverão, detalha Feinberg.
A maioria das pacientes necessita de pelo menos duas ou três transferências antes de engravidar, acrescenta McLean.
Os médicos agora tentam limitar o número de vezes que recuperam óvulos e estimulam os ovários de uma paciente porque isso acarreta riscos à saúde e custos consideráveis, observa ele.
Mas as famílias podem optar por limitar o número de óvulos fertilizados para criar embriões e, antes de se submeterem à Fertilização in Vitro, falar com o seu médico sobre as suas considerações morais e éticas pessoais, esclarece McLean.
Fonte: Fertilização in Vitro: o que é e quando é recomendada? | CNN Brasil